Адгезия что это? И когезия
Приветствую. Меня зовут Роман, и это мой авторский блог ✍️ про укладку плитки и мозаики. Обучение + кураторство 👉 ЗДЕСЬ. Если нужен быстрый ответ по теме блога, то вам сюда 👉 ПРОФИЛЬНЫЕ КОНСУЛЬТАЦИИ
А вы знали, что в строительстве, в частности у штукатуров, есть такое понятие, как штукатурный обрызг? Его ещё называют “адгезионный слой”. Как думаете, что это такое и для чего?
Не буду томить.
По сути, задача этого слоя — создание шероховатой высокоадгезионной поверхности — это делается для того, чтобы цементная штукатурка, которая ляжет сверху, хорошенько приклеилась. Кстати, в процессе высыхания она благополучно набирает не только адгезионную но и когезионную прочность.
То что набрызгано — обрызг, там, где видны следы от гладилки — предварительное промазывание “насдир” для улучшения адгезии (подробнее ниже)- Что это такое — адгезия основания? Например: адгезия эпоксидного клея к стеклу?
- Можно ли её как-нибудь усилить?
- Что такое когезия? Например: что такое когезия плиточного клея?
- А когезионные свойства у материала и можно ли как-то улучшить когезию?
Давайте разбираться
🧐👇
📑 Содержание:
Что такое когезия в строительстве?
Если просто, когезия — это связь между молекулами внутри материала. По сути, речь идёт о прочности материала (тела), например, плиточного клея, и его способности противостоять внешнему воздействию — “на разрыв”, если быть совсем точным “на когезионный разрыв”.
По сути, речь идёт о прочности материала (тела), например, плиточного клея, и его способности противостоять внешнему воздействию — “на разрыв”, если быть совсем точным “на когезионный разрыв”.
Разумеется, это речь идёт о “телах”, которые уже успели набрать свою заложенную прочность😉.
Отсюда и название: когезионная прочность, или такое понятие, как “степень когезионной прочности”.
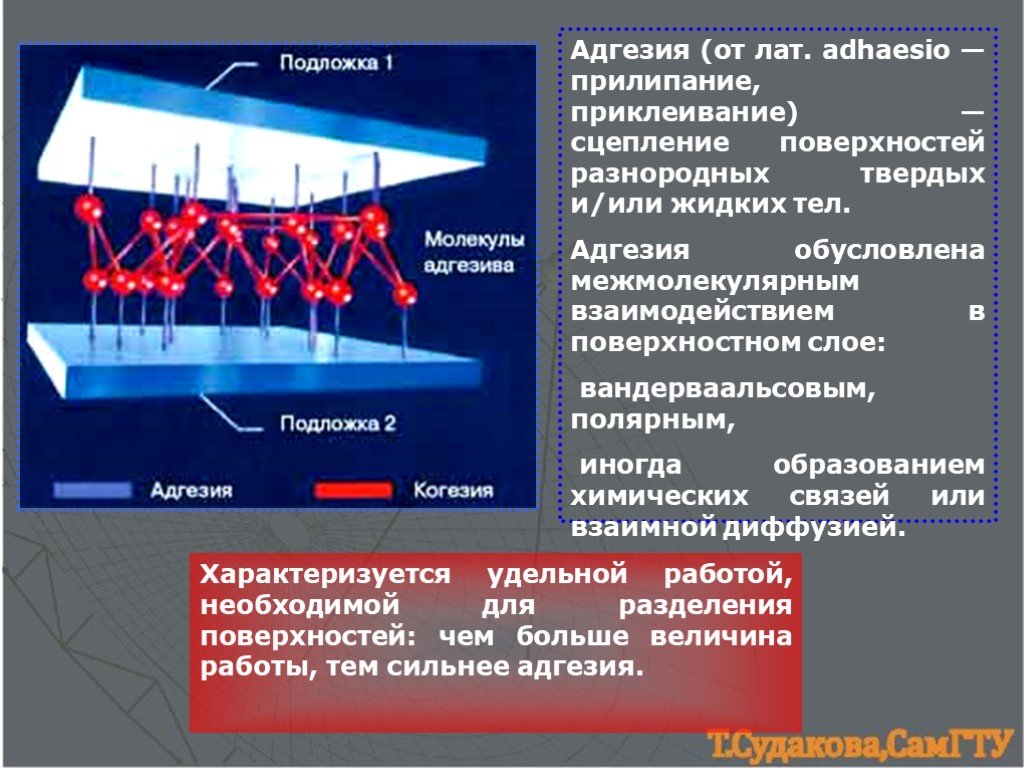
Разница между адгезией и когезией хорошо видна на этом изображении:
Связи, которые отображены голубым — когезия, оранжевым — адгезия.Справка из википедии: Когезионный (англ. cohesion от лат. cohaesus — это значит «связанный», «сцепленный»).
Что такое адгезия в строительстве?
Адгезия — это сцепление поверхностей разнородных твёрдых и/или жидких тел. Я бы ещё добавил – на молекулярном уровне.
Например, плиточного клея с плиткой и штукатуркой или цементной гидроизоляцией. Как раз недавно сцеплял клей ceresit cm17 с цементной гидроизоляцией и плиткой 1200*600:
Важно перед тем, как был нанесён клей основания (штукатурка и плитка) были тщательно промазаны плиточным клеем. Это как раза для улучшения адгезии.
Это как раза для улучшения адгезии.Или адгезия герметика с плиткой:
Этот скрин я сделал из видео Шайтера Андрея. Кстати, очень рекомендую к просмотру — много любопытного узнаете о герметике.В ролике есть фрагмент, где наглядно видно как герметик рвётся при когезионном разрыве:
Справка из википедии: Адгезия (от лат. adhaesio — это прилипание)
Иными словам, когда упоминают про адгезию, то имеют ввиду прочность сцепления в местах соприкосновения разных материалов, а когда когезию — рвётся в середине (теле) материала.
Думаю по описанию хорошо видно, что когда говорят о когезии, то речь не идёт о прилипании.
Наглядный пример из жизни: штукатурка + плиточный клей + плитка
На самом деле все, кто трудиться на стройке очень часто сталкиваются с проявлениями этих видов разрушений.
Случай первый — когда когезионная прочность сильнее, чем адгезионная прочность:Представим себе, что нам понадобилось демонтировать уложенную пару недель назад плитку.
Берём для этого широкое зубило, обычный молоток:
Этого друга можно смело награждать всевозможными почестями. Чего только он не видел — и барбекю с печами им клали и стены ломали…)Зубило, шириной 10 см иногда очень выручает. Как только встретил его в Кастораме, сразу же купил.Вставляем зубило между плиткой и основанием и начинаем производить удары, тем самым прилагая усилие “на разрыв”. Т.е мы не сверху бьём, а сбоку, иначе плитка разобьётся и эксперимент будет провален.
Если в этом случае плитка вместе с клеем легко отпадает от стяжки или штукатурки, не оставляя там следов или наоборот — весь клей остался на основании, а плитку даже и чистить не надо, то в этом случае когезионное сцепление было крепче, чем адгезионное. Т.е. когезия в данном случае проиграла.
Т.е. когезия в данном случае проиграла.
Если в нашем примере остаётся клей и на штукатурке и на плитке и разрыв идёт в слое плиточного клея, то здесь когезия была слабее нежели адгезия.
На фото яркий пример когезионного разрыва или “когезионного разрушения” внутри слоя — вся штукатурка, как видите на плитке.
На самом деле, в данном случае она осыпалась даже тогда, когда я просто проводил по ней пальцем… Да, и такое бывает…
Можно ли усилить адгезию и когезию?
Усиление адгезии
Для этого как раз и существуют специальные пропитки, те же самые грунтовки для предварительной обработки поверхности. Например, популярная на сегодня Грунтовка ceresit ct17:
Или адгезионная добавка для штукатурки. К примеру адгезионную добавку ceresit cc81 я использовал при штукатурке лестницы:
На самом деле зачастую, чтобы улучшить адгезию достаточно просто тщательно пропылесосить + перед тем как штукатурить или наносить смесь — тщательно промазать оcнование (на сдир), а там нед всякого рода углубления руками в перчатках + соблюдать все технологические процессы и условия при проведении работу.
Поверьте, если в жару попытаться приклеить плитку на клей, который уже минут пять, как “начёсан” — ничего хорошего из этого не получится (на солнце и в ветреную погоду влага очень быстро испаряется из плиточного клея и верхний слой выветривается и адгезия плитки с клеем сильно уменьшится).
Разумеется, существуют специальные клея с увеличенным открытым временем, но это не панацея.
Улучшение когезии
Существуют пластификаторы на подобии этого:
Которые помимо всего прочего увеличивают прочность цементной смеси + придают ей гидрофобные свойства, чтобы готовый бетон меньше впитывал влагу.
Пример параметров адгезии плиточного клея LITOSTONE K99 (БЕЛЫЙ):
| Характеристика | Единица меры адгезии | Параметр |
|---|---|---|
Адгезия (прочность клеевого соединения) после выдерживания в воздушно-сухой среде. | МПа | ≥1,0 |
| Адгезия (прочность клеевого соединения) после циклического замораживания и оттаивания.  | МПа | ≥1,0 |
| Адгезия (прочность клеевого соединения после выдерживания при высоких температурах | МПа | ≥1,0 |
| Адгезия (прочность клеевого соединения) после выдерживания в водной среде | МПа | ≥1,0 |
| Адгезия (прочность клеевого соединения после выдерживания в воздушно-сухой среде в течение 6 часов | МПа | ≥0,5 |
Методы испытания адгезии и когезии (ГОСТ-56387-2018)
Расскажу на примере плиточного клея и ГОСТ-56387-2018. У самого простого плиточного клей класса C0, адгезия после выдерживания приклеенной на него плитки в комнатных условиях 27 суток должна быть не менее 0,5 MPa.
Проверка:
Сверху к плитке приклеивают штамп с помощью высокопрочного клея (эпоксидного например), далее через 24 часа к штампу прикладывают нагрузку с постоянной скоростью возрастания (250 ± 50) Н/с.
После чего смотрят, где порвётся. Разрушения делят на два уже знакомых Вам типа:
Адгезионные разрушения:Разрушения могут быть на границе между поверхностями клеевого раствор и основания:
Разрушение между поверхностями керамической плитки и клеевого раствора:
В случае если оторвался штамп от самой плитки, то опыт повторяют:
Когезионные разрушения:В данном случае когезия нарушается внутри слоя клеевого раствора:
Здесь когезия нарушается внутри керамической плитки:
Разрушение происходит внутри слоя клеевого раствора:
Подробнее о том как обрабатывают результаты и производят вычисления читайте в ГОСТ-56387-2018)
Адгезивность материала
Из всего вышесказанного можно предположить, что адгезивность материала — это степень надёжности его сцепления с другим материалом. Насколько крепко держится.
Насколько крепко держится.
Адгезия в медицине
В биологии под адгезионными свойствами клетки понимают комплекс ее характеристик, определяющий способность устанавливать и поддерживать контакты (связь) с другими клетками и (или) неживым субстратом.
В результате адгезионных взаимодействий происходит образование межклеточного контакта — специализированной структуры, которую можно рассматривать как системообразующий элемент при переходе от клеточного к тканевому уровню организации.
Межклеточный контакт представляет собой своеобразную органеллу клетки, состоящую из плазматических мембран и специальных структур контактирующих клеток. Предполагают, что адгезионные взаимодействия играют чрезвычайно важную роль в таких процессах, как морфогенез ткани, регуляция деления клеток, малигнизация.
Подробнее здесь
На сегодня всё). Всем добра!)
Когезия и адгезия
Явления смачивания
и растекания тесно связаны с действием
сил когезии и адгезии.
Когезией называют сцепление однородных молекул, атомов или ионов, которое включает все виды межмолекулярного и межатомного притяжения внутри одной фазы.
Когезия определяет существование веществ в конденсированном (твердом и жидком) состоянии. Такие состояния характеризуются высокой когезией. Газообразные вещества обладают малой когезией.
Адгезия (прилипание) – это молекулярное притяжение между поверхностями двух соприкасающихся разнородных твердых или жидких фаз. Адгезия является причиной склеивания двух разных веществ за счет действия физических или химических межмолекулярных сил.
Количественно когезию и адгезию характеризуют величиной работы когезии Wc и работы адгезии Wa.
Wc = 2 · σ
Работа адгезии – это работа, затрачиваемая на отрыв молекул одной фазы от молекул другой фазы
Wa = σА + σВ + σАВ
σА – поверхностное натяжение на границе вещества А с воздухом
σВ – поверхностное натяжение на границе вещества В с воздухом
σАВ — поверхностное натяжение на границе веществ А и В
Из уравнения видно, что работа адгезии тем больше, чем больше поверхностное натяжение каждой из фаз на границе с воздухом и чем меньше поверхностное натяжение на границе раздела между фазами А и В.
Рассматриваемые
явления играют большую роль в таких
процессах, как смачивание материалов,
нанесение лакокрасочных и гальванических
покрытий, получение материалов на основе
связующих и наполнителей (бетон, резина,
стеклопластики и др. ), крашение, печатание,
сварка и металлов.
), крашение, печатание,
сварка и металлов.
Учитываются и используются адгезия и когезия в технологии лекарств, поскольку они влияют на взаимодействие компонентов в сложных лекарственных формах, на распадаемость таблеток, прочность покрытия их оболочками, на процессы растворения и в конечном итоге на эффективность терапевтического действия.
Заключение
К явлениям адсорбции
близки явления смачивания и адгезии,
определяющиеся интенсивностью
взаимодействия между молекулами разных
веществ. Количественными характеристиками
смачивания являются краевой угол и
теплота смачивания. По способности
поверхностей избирательно смачиваться
водой, их классифицируют на гидрофильные
(θ < 90
Когезию и адгезию количественно оценивают работой, необходимой для разрыва связей между молекулами данной фазы или разных фаз.
Вопросы для самоконтроля
Чем обусловлено смачивание?
Что называется краевым углом смачивания? Как его определяют экспериментально?
Какие поверхности называют гидрофильными, гидрофобными?
Как можно осуществить инверсию смачивания?
Чем отличается когезия от адгезии?
Адгезия и когезия – разница и сравнение
Когезия – это свойство одинаковых молекул (одного и того же вещества) прилипать друг к другу за счет взаимного притяжения.
Сравнительная таблица
| Адгезия | Когезия | |
|---|---|---|
| Компоненты | Разнородные молекулы | Подобные молекулы |
| Эффект | Капиллярное действие, мениск | Поверхностное натяжение, капиллярное действие и мениск |
Эффекты когезии и адгезии
Поверхностное натяжение
Поверхностное натяжение является результатом сил сцепления между соседними молекулами.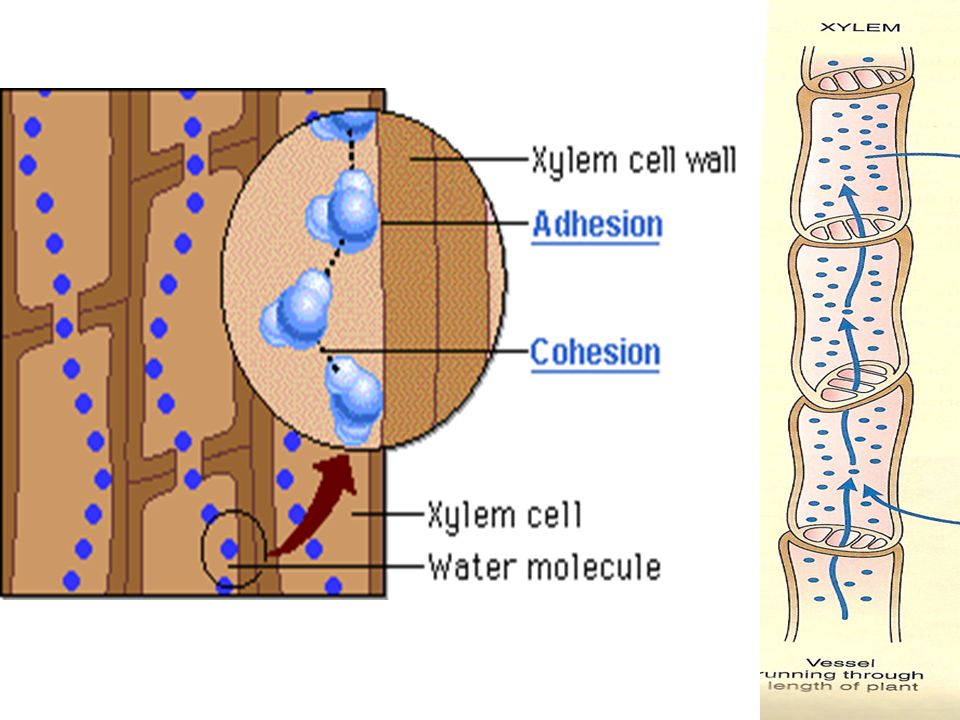 Молекулы в объеме жидкости одинаково притягиваются соседними молекулами во всех направлениях. Но поверхностные молекулы не имеют молекул со всех сторон. Следовательно, они втягиваются внутрь, заставляя жидкость сжиматься, образуя поверхность с минимальной площадью, сферу. Следовательно, капли воды имеют сферическую форму.
Молекулы в объеме жидкости одинаково притягиваются соседними молекулами во всех направлениях. Но поверхностные молекулы не имеют молекул со всех сторон. Следовательно, они втягиваются внутрь, заставляя жидкость сжиматься, образуя поверхность с минимальной площадью, сферу. Следовательно, капли воды имеют сферическую форму.
Молекулы воды слипаются на вощеной бумаге, потому что поверхностное натяжение больше, чем силы сцепления между бумагой и молекулами воды.
Поверхностное натяжение воды позволяет объектам тяжелее нее плавать по ней. Когда молекулы воды не прилипают к объекту (не смачивается) и вес объекта меньше сил поверхностного натяжения.
Мениск
Вогнутый и выпуклый мениск. Мениск вогнут, когда силы сцепления больше, чем силы сцепления. например вода. Он выпуклый, когда сцепление сильнее. например ртуть
например ртуть
Изогнутая поверхность жидкости внутри сосуда называется мениском.
- Когда силы сцепления между молекулами жидкости больше, чем силы сцепления между жидкостью и стенкой сосуда, поверхность жидкости выпуклая. Например, Меркурий в контейнере.
- Когда силы сцепления между жидкостью меньше, чем силы сцепления между жидкостью и контейнером, поверхность изгибается вверх. Например, вода в стеклянной посуде.
- Когда силы сцепления и силы сцепления равны, поверхность горизонтальна. Например, дистиллированная вода в серебряном сосуде.
Капиллярное действие
Капиллярное действие является результатом когезионных и адгезионных сил. Когда жидкость течет через узкое пространство, когезионная и адгезионная силы действуют вместе, поднимая ее против естественной силы гравитации. Смачивание бумажного полотенца, стекание воды от корней к верхушке растения — вот несколько примеров капиллярного действия.
Ртуть лучше сцепляется со стеклом, чем слипается.
Когезия заставляет воду образовывать капли, поверхностное натяжение делает их почти сферическими, а адгезия удерживает капли на месте.
Области применения
Адгезия используется для надлежащего функционирования клея, краски, смолы, цемента, чернил и т. д. Адгезионные и когезионные силы вместе вызывают капиллярное действие, которое является принципом, используемым в фитилях ламп. Синтетические волокна используют влагоотведение для удаления пота с кожи.
Ссылки
- Сплоченность – выдержка из Общая наука
- Википедия:Слипание
- Wikipedia:Cohesion_(химия)
- Wikipedia:Surface_tension#Причины
- Википедия:Капиллярное действие
- Силы сцепления и сцепления — ThinkQuest.org
- Подписаться
- Поделиться
- Укажите
- Авторы
Поделитесь этим сравнением:
Если вы дочитали до этого места, подписывайтесь на нас:
«Сплоченность против сплоченности».
Силы сцепления и сцепления — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 1499
Силы сцепления и адгезии связаны с объемными (или макроскопическими) свойствами, и, следовательно, эти термины неприменимы к обсуждению атомарных и молекулярных свойств. Когда жидкость вступает в контакт с поверхностью (например, со стенками градуированного цилиндра или столешницей), на нее действуют как силы сцепления, так и силы сцепления. Эти силы управляют формой, которую принимает жидкость. Из-за действия сил сцепления жидкость на поверхности может растекаться, образуя тонкую, относительно однородную пленку по поверхности, этот процесс известен как смачивание.
Адгезионные и когезионные силы
Термин «когезионные силы» является общим термином для коллективных межмолекулярных сил (например, водородных связей и сил Ван-дер-Ваальса), ответственных за объемное свойство жидкостей, сопротивляющихся разделению. Именно эти силы притяжения существуют между молекулами одного и того же вещества. Например, дождь падает каплями, а не мелким туманом, потому что вода обладает сильным сцеплением, которое плотно стягивает ее молекулы, образуя капли. Эта сила стремится объединить молекулы жидкости, собирая их в относительно большие кластеры из-за неприязни молекул к окружающей среде.
Аналогичным образом, термин «силы сцепления» относится к силам притяжения между разнородными веществами, таким как механические силы (слипание друг с другом) и электростатические силы (притяжение из-за противоположных зарядов). В случае жидкого смачивающего агента адгезия заставляет жидкость прилипать к поверхности, на которой она находится. Когда воду наливают на чистое стекло, она имеет тенденцию растекаться, образуя тонкую равномерную пленку на поверхности стекла. Это связано с тем, что силы сцепления между водой и стеклом достаточно сильны, чтобы вытащить молекулы воды из их сферического образования и удержать их на поверхности стекла, тем самым избегая отталкивания между подобными молекулами.
В случае жидкого смачивающего агента адгезия заставляет жидкость прилипать к поверхности, на которой она находится. Когда воду наливают на чистое стекло, она имеет тенденцию растекаться, образуя тонкую равномерную пленку на поверхности стекла. Это связано с тем, что силы сцепления между водой и стеклом достаточно сильны, чтобы вытащить молекулы воды из их сферического образования и удержать их на поверхности стекла, тем самым избегая отталкивания между подобными молекулами.
Макроскопические эффекты когезионных и адгезионных сил
Когда жидкость помещается на гладкую поверхность, относительная сила когезионных и адгезионных сил, действующих на эту жидкость, определяет форму, которую она примет (и будет ли она смачивать поверхность или нет ). Если силы сцепления между жидкостью и поверхностью сильнее, они будут тянуть жидкость вниз, заставляя ее смачивать поверхность. Однако, если силы сцепления между самой жидкостью сильнее, они будут препятствовать такому слипанию и заставят жидкость сохранять сферическую форму и выпуклость на поверхности.
Случай I: Мениск
Мениск представляет собой кривизну поверхности жидкости внутри сосуда, такого как мерный цилиндр. Однако, прежде чем мы объясним, почему у некоторых жидкостей мениск вогнут вверх, а у других мениск вогнут вниз, мы должны понять силы сцепления при работе поверхностного натяжения. Вода, например, представляет собой полярную молекулу, состоящую из частичного положительного заряда атомов водорода и частичного отрицательного заряда кислорода. Таким образом, в жидкой воде частичный положительный заряд каждой молекулы притягивается к частичному отрицательному заряду соседней молекулы. Это источник сил сцепления в воде. Молекулы воды, погруженные в жидкость, затем вытягиваются и равномерно выталкиваются во всех направлениях, не создавая чистого притяжения. Между тем, молекулы на поверхности жидкости, лишенные сил притяжения в восходящем направлении, таким образом охватывают результирующее притяжение вниз.
Как тогда эта сила сцепления создает и вогнутую вверх, и вогнутую вниз поверхность? Ответ заключается в его отношении к силам сцепления между молекулами воды и поверхностью сосуда. Когда сила сцепления жидкости больше, чем сила сцепления жидкости со стенкой, жидкость вогнута вниз, чтобы уменьшить контакт с поверхностью стенки. Когда сила сцепления жидкости со стенкой больше, чем сила сцепления жидкости, жидкость сильнее притягивается к стенке, чем ее соседи, вызывая вогнутость вверх.
Когда сила сцепления жидкости больше, чем сила сцепления жидкости со стенкой, жидкость вогнута вниз, чтобы уменьшить контакт с поверхностью стенки. Когда сила сцепления жидкости со стенкой больше, чем сила сцепления жидкости, жидкость сильнее притягивается к стенке, чем ее соседи, вызывая вогнутость вверх.
Случай II: Слезы вина
В встряхиваемых бокалах с вином капли вина как бы «плавают» над мениском жидкости и образуют «слезы». Это вековое явление является результатом поверхностного натяжения и когезионных и адгезионных сил. Спирт более летуч, чем вода. В результате «испарение спирта создает градиент поверхностного натяжения, поднимающий тонкую пленку вдоль стенок бокала» (Адамсон). Этот процесс называется «солютным эффектом Марангони». 2 За счет сил сцепления часть воды прилипает к стенкам стакана. «Слезы» образуются из-за сил сцепления внутри воды, удерживающих ее вместе. Важно отметить, что градиент поверхностного натяжения является «движущей силой движения жидкости» (Гульотти), но фактическое образование разрывов является результатом когезионных и адгезионных сил.
Задачи
- Назовите два примера, где сила сцепления преобладает над силой сцепления и наоборот.
- В стеклянном градуированном цилиндре вода представляет собой вогнутый вверх мениск. Однако, когда вода заполнена до кончика цилиндра, уровень воды может поддерживаться выше стенки цилиндра, не выливаясь, напоминая вогнутый вниз мениск. Используйте принципы когезионных и адгезионных сил, чтобы объяснить эту ситуацию.
- Объясните, почему водомер может скользить по воде, зная сцепление в воде.
- Предложите различные типы сил, на которых могут основываться силы сцепления.
Ответы
- Когда сила сцепления больше, чем сила сцепления: вогнутый мениск, вода образует капли на поверхности.
 Когда сила сцепления больше, чем сила сцепления: мениск вогнут вниз, поверхности покрыты смачивающим веществом, последние капли жидкости в бутылке всегда отказываются выходить.
Когда сила сцепления больше, чем сила сцепления: мениск вогнут вниз, поверхности покрыты смачивающим веществом, последние капли жидкости в бутылке всегда отказываются выходить. - Поскольку вода образует вогнутый мениск, сцепление молекул со стеклом сильнее, чем сцепление между молекулами. Однако при отсутствии силы сцепления (когда вода достигает кончика стакана) сила сцепления остается. Таким образом, сила сцепления сама по себе доказывает, что она еще может удерживать себя на месте, не вытекая из цилиндра. Этот пример подчеркивает важность того, что силы сцепления и силы сцепления не просто компенсируют друг друга, но именно разница между ними определяет характеристики жидкости.
- Эта задача еще раз обращается к концепции поверхностного натяжения. Поскольку сцепление воды основано на слабых межмолекулярных силах воды, когда водомерка выходит на поверхность, потребуется дополнительная энергия, чтобы преодолеть эти связи, чтобы увеличить площадь поверхности.
 Более того, поскольку гравитационное притяжение водомерки не может преодолеть энергию активации, чтобы разрушить эти межмолекулярные силы, водомерка может свободно скользить по воде.
Более того, поскольку гравитационное притяжение водомерки не может преодолеть энергию активации, чтобы разрушить эти межмолекулярные силы, водомерка может свободно скользить по воде. - Дополнительная форма, образование химических связей, слабые межмолекулярные силы, такие как Н-связь или силы Ван-дер-Ваальса.
Ссылки
- Петруччи и др. Общая химия: принципы и современные приложения: AIE (твердый переплет). Река Аппер-Сэдл: Пирсон / Прентис-Холл, 2007 г. .
- Гуглиотти, Маркос. «Слезы вина». Журнал химического образования 81.1 (2004): 67-68. Веб. 9 марта 2010 г.
- Адамсон, А. В.; Гаст, А. П. Физическая химия поверхностей , 6-е изд.; Джон Уайли и сыновья: Нью-Йорк, 1997; стр. 371.
Авторы и ссылки
- Кэмерон Трейси, Лин Се, Ирэн Лим, Генри Ли
Cohesive and Adhesive Forces распространяется под лицензией CC BY и был создан, изменен и/или курирован LibreTexts.

 Когда сила сцепления больше, чем сила сцепления: мениск вогнут вниз, поверхности покрыты смачивающим веществом, последние капли жидкости в бутылке всегда отказываются выходить.
Когда сила сцепления больше, чем сила сцепления: мениск вогнут вниз, поверхности покрыты смачивающим веществом, последние капли жидкости в бутылке всегда отказываются выходить. Более того, поскольку гравитационное притяжение водомерки не может преодолеть энергию активации, чтобы разрушить эти межмолекулярные силы, водомерка может свободно скользить по воде.
Более того, поскольку гравитационное притяжение водомерки не может преодолеть энергию активации, чтобы разрушить эти межмолекулярные силы, водомерка может свободно скользить по воде.